美国科学家克服了微型器官产生中的一个主要障碍,可以对细胞进行编程以使其具有所需的形状,而不是依靠3D打印或外部“支架”。
这种“由内而外”的方法在《细胞系统》杂志上的一篇论文中进行了描述,它可能标志着微型心脏,肾脏和大脑在实验室工作台上的生长方式发生了转变-一种用于研究可能一天导致个性化器官移植。
该团队由美国Gladstone研究所的生物工程师Todd McDevitt领导,受到持续不断的问题的困扰,这些问题涉及生产微型器官(例如3D打印)的最新技术。牢房将不会留在原地。
当科学家获取一个人的皮肤细胞,并使用正确的混合剂将其转变为“诱导的多能干细胞”时,便开始制造微型器官或“类器官”。这种IPS细胞是生物学的空白对照,能够变成几乎任何类型的细胞。
举例来说,将其长成迷你肾脏,就可以在实验室工作台上的盘子中繁殖肾脏疾病并进行治疗。但是,该模型的可信度取决于细胞的物理组织。为了模仿真正的肾脏,通常使用3D打印。
但是细胞,就像不守规矩的青少年一样,有自己的头脑,并且经常会偏离其印刷位置。
McDevitt的团队希望拥有这些细胞的头脑,因此控制了两个基因,这些基因共同构成操纵杆,指导细胞如何组织。
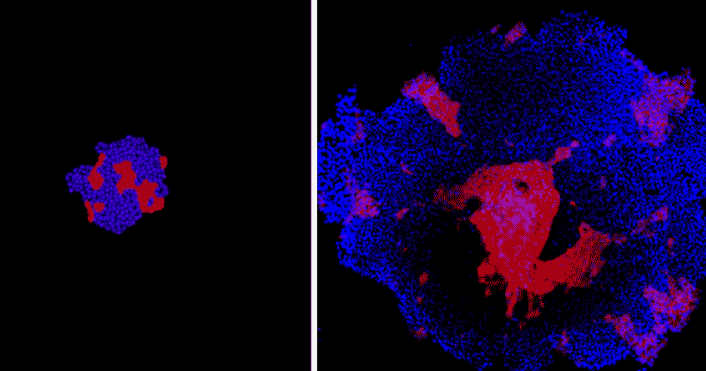
CDH1和ROCK1在导致一组单元最终配置的复杂动作中占有重要地位。该对影响细胞之间的粘性和排斥力,使它们呈球形的表面张力以及整体迁移速度。研究人员使用编辑工具CRISPR在细胞团进化的不同阶段敲除了这两个基因。他们的目标是制作牛眼图案,这种形状在人类发育中很常见,包括在早期胚胎形成中。
为了检测这种吸气模式,他们进行了另一项调整-在CDH1和ROCK1被中和时使细胞发出荧光。
但有一个问题。
将基因可能被剔除的所有潜在时间点,要靶向的细胞比例以及许多其他变量考虑在内,研究人员计算出,他们需要进行近9000次试错实验。
因此,他们呼吁AI。他们训练了机器学习模型,以计算实现梦想形状所需的基因敲除的精确模式。
波士顿大学生物信息学计划的合著者Demarcus Briers说:“机器学习可以根据您的观看历史预测您喜欢的电影,但是通过模仿它们,也可以对生物系统产生新的见解。”
“我们的机器学习模型使我们能够预测干细胞组织自身的新方式,并提供有关如何在实验室中重新创建这些预测的说明。”
从字面上看,该模型非常有用,它使团队能够产生他们所瞄准的同心圆状细胞。
McDevitt说:“我们已经展示了如何利用干细胞的内在能力进行组织。”“这为我们提供了一种工程化组织的新方法,而不是一种打印方法,在该方法中,您试图将细胞物理地逼入特定的结构。”
 教育新闻网
教育新闻网














